"Las especificaciones de este lote no corresponde a lo que venía en los certificados de calidad, lo que ha obligado a devolver los lotes, y la empresa va a cambiarlos", dijo en rueda de prensa el director del Centro de Coordinación de Alertas Sanitarias, Fernando Simón.
Así lo explicó Simón tras ser preguntado por un artículo del diario El País donde se cuestionaba la fiabilidad de una partida de 340.000 kits adquiridos en China.
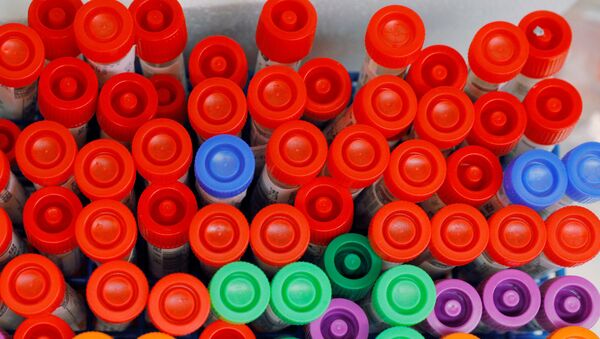
El primer envío de 9.000 pruebas resultó tener "una sensibilidad del 30%, cuando debería ser superior al 80%", reveló al diario uno de los microbiólogos españoles que participaron en la validación de los test.
A raíz de estas informaciones, que fueron reproducidas por varios medios de comunicación españoles, la Embajada de China en España aseguró que la empresa en cuestión no contaba con licencia para vender este tipo de herramientas médicas.
"Shenzhen Bioeasy Biotechnology no ha conseguido todavía la licencia oficial de la Administración Nacional de Productos Médicos de China para vender sus productos", comunicó la Embajada a través de las redes sociales.
La Embajada precisó que los productos vendidos por esta compañía no están incluidos en ninguna de las donaciones de material sanitario y médico a España por parte del Gobierno de China y el gigante Alibaba.
Las autoridades diplomáticas explicaron además que el Ministerio de Comercio de China "ofreció a España una lista de proveedores clasificados" en la que no figuraba esta empresa.
Los test de detección del coronavirus empleados por los laboratorios españoles utilizan la técnica del PCR, que no ofrece conclusiones hasta varias horas más tarde de tomar la muestra, mientras que las pruebas rápidas dan resultados en 10 o 15 minutos.
El Gobierno movilizó en las últimas semanas grandes cantidades de material médico procedente del extranjero, entre las cuales se encuentran más de 640.000 unidades de este tipo de pruebas.